O deslumbrante experimento de oxidação da dipirona
Segunda-feira, 10 de novembro de 2025
Última modificação: Segunda-feira, 10 de novembro de 2025
A dipirona é um medicamento analgésico e antitérmico. Sua oxidação, em meio ao oxidante hipoclorito de sódio, presente na água sanitária comercial, gera mudanças de cor do meio reacional com o tempo. Inicialmente, forma-se uma mistura de cor azul-escura. Com o tempo, observa-se uma tonalidade esverdeada que passa, em seguida, para uma coloração amarela (Figura 1). Dependendo das condições experimentais, a liberação de gases (N2 e CO2) pode ser evidenciada.
Figura 1 – Formação das diferentes cores ao longo da oxidação da dipirona

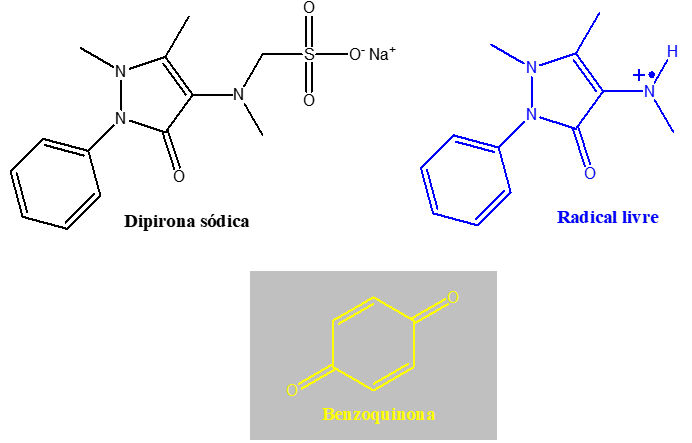
Na reação, seu sal (dipirona sódica (Figura 2)) atua na reação como um reagente redutor, sendo o seu grupo sulfonometila oxidado e removido. O hipoclorito de sódio (NaClO), por sua vez, é o reagente oxidante que se converte em cloreto de sódio (NaCl) ao final da reação. Um dos compostos intermediários da reação é um radical livre (Figura 2), pouco estável, de coloração azul, percebido visualmente em seu período curto de existência. Como um dos produtos da reação é a benzoquinona (Figura 2), de coloração amarela intensa, tem-se a formação da cor esverdeada até o desaparecimento do radical livre, onde o meio reacional permanece amarelo devido à benzoquinona.
Figura 2 – Fórmulas estruturais da dipirona sódica, do radical livre formado na reação e da benzoquinona
Outro ponto interessante sobre o experimento é o período viável de visualização do radical livre, considerando sua instabilidade. Isso ocorre, pois a ressonância eletrônica reduz em parte a instabilidade devido à deslocalização do elétrons desemparelhado.
Por fim, destaca-se que, por mais que o assunto seja interessante para os profissionais de química, o experimento não deve ser feito fora dos laboratórios especializados e sem a supervisão de um docente responsável. Isso, pois a água sanitária é uma mistura básica contendo um agente oxidante forte, além da benzoquinona, formaldeído, possíveis cloraminas etc. serem produtos que podem causar danos à saúde humana.

 Serviço de e-mail
Serviço de e-mail